Diferencia entre revisiones de «Inyección intracitoplasmática de espermatozoides»
| Línea 26: | Línea 26: | ||
<ref>{{cita publicación|apellido=Bonduelle|nombre=M.|coautores=Van Assche, E., Joris, H., Keymolen, K., Devroey, P., Van Steirteghem, A., Liebaers, I.|título=Prenatal testing in ICSI pregnancies: incidence of chromosomal anomalies in 1586 karyotypes and relation to sperm parameters|publicación=Human Reproduction|año=2002|volumen=17|páginas=2600-2614}}</ref> | <ref>{{cita publicación|apellido=Bonduelle|nombre=M.|coautores=Van Assche, E., Joris, H., Keymolen, K., Devroey, P., Van Steirteghem, A., Liebaers, I.|título=Prenatal testing in ICSI pregnancies: incidence of chromosomal anomalies in 1586 karyotypes and relation to sperm parameters|publicación=Human Reproduction|año=2002|volumen=17|páginas=2600-2614}}</ref> | ||
analizan el riesgo de una anormalidad cromosómica nueva, no presente en los gametos; encuentran que es de 1.6% para los generados por ICSI frente a un 0.5% de los concebidos. Estas alteraciones fetales de novo consisten fundamentalmente en un incremento del número de cromosomas sexuales, que cursan con esterilidad, y sus manifestaciones fenotípicas son indetectables al nacer y en los primeros años de vida. Se ha relacionado la incidencia de alteraciones en los niños de ICSI con alteraciones del cromosoma Y paterno <ref>{{cita publicación|apellido=Yukiko|nombre=Katagiri|coautores=Queenie V Neri, Takumi Takeuchi, Peter N Schlegel, Wael A Megid, Marijo Kent-First, Zev Rosenwaks, Gianpiero D Palermo|título=Y chromosome assessment and its implications for the development of ICSI children|publicación=Reproductive BioMedicine Online|año=2004|volumen=8|número=3|páginas=307-318|doi=10.1016/S1472-6483(10)60911-X|url=http://download.journals.elsevierhealth.com/pdfs/journals/1472-6483/PIIS147264831060911X.pdf}}</ref> | |||
Actualmente, las técnicas de biomedicina están permitiendo la disección de los genes del cromosoma Y que se requieren para la fertilidad masculina; este análisis permitirá un mejor diagnostico de la causa de infertilidad y permitiría la posibilidad de una información rigurosa a quienes acuden a la ICSI y valorar con ello las malformaciones esperables en los hijos. | Actualmente, las técnicas de biomedicina están permitiendo la disección de los genes del cromosoma Y que se requieren para la fertilidad masculina; este análisis permitirá un mejor diagnostico de la causa de infertilidad y permitiría la posibilidad de una información rigurosa a quienes acuden a la ICSI y valorar con ello las malformaciones esperables en los hijos. | ||
Revisión del 00:21 29 oct 2012
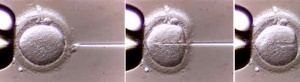
La inyección introcitoplasmática de especmatozoides (Intracytoplasm sperm injection - ICSI) es una técnica de reproducción asistida extracorpórea que consiste en la inyección de un solo espermatozoide en el citoplasma del óvulo.
La esterilidad masculina tiene como indicación del uso de la ICSI. Basta que haya algún espermatozoide en el semen, el epidídimo o el testículo. Comenzó a utilizarse en 1992 en Bélgica.
Aunque es una técnica muy difundida por su efectividad, se ha observado que esta facilidad para conseguir la fecundación lleva aparejado el aumento de riesgo de enfermedades genéticas en el embrión.
Un informe exhaustivo de febrero de 2005
[1]publicados en todos los países sobre la salud de los niños generados por FIV e ICSI y
pone de manifiesto que estos últimos tienen más riesgo de tres a cuatro veces mayor
que los concebidos naturalmente de anormalidades crosomómicas. En buena medida las
alteraciones son heredadas de los gametos paternos.
Los trabajos del equipo de Bonduelle
[2] analizan el riesgo de una anormalidad cromosómica nueva, no presente en los gametos; encuentran que es de 1.6% para los generados por ICSI frente a un 0.5% de los concebidos. Estas alteraciones fetales de novo consisten fundamentalmente en un incremento del número de cromosomas sexuales, que cursan con esterilidad, y sus manifestaciones fenotípicas son indetectables al nacer y en los primeros años de vida. Se ha relacionado la incidencia de alteraciones en los niños de ICSI con alteraciones del cromosoma Y paterno [3]
Actualmente, las técnicas de biomedicina están permitiendo la disección de los genes del cromosoma Y que se requieren para la fertilidad masculina; este análisis permitirá un mejor diagnostico de la causa de infertilidad y permitiría la posibilidad de una información rigurosa a quienes acuden a la ICSI y valorar con ello las malformaciones esperables en los hijos.
El hecho de introducir directamente el espermatozoide en el óvulo ocasiona que también se introduzcan estructuras espermáticas que pueden transmitir al ovocito defectos cromosómicos presentes en el espermatozoide. El espermatozoide que penetra no es el mejor –como ocurre en el proceso natural–, lo que conlleva un aumento de riesgos para el nuevo individuo.
También se ha constatado un aumento de la incidencia de gemelación del cigoto, y consecuentemente del número de gemelos en los nacimientos.
En el caso de plantearse acudir a la ICSI, además de las consideraciones éticas que deben tenerse en cuenta en la utilización general de las TRA, debería contarse con este aumento de los riesgos para el embrión y para la madre.
Referencias
- ↑ Marjoribanks, J.; Farquhar, C., Marshall C (2005). Systematic review of the health risks to the mother, child and family associated with the use of intracytoplasmic sperm injection (ICSI). Report to the Ministry of Health from the New Zealand Guidelines Group undertaken by the Cochrane Menstrual Disorders and Subfertility.
- ↑ Bonduelle, M.; Van Assche, E., Joris, H., Keymolen, K., Devroey, P., Van Steirteghem, A., Liebaers, I. (2002). «Prenatal testing in ICSI pregnancies: incidence of chromosomal anomalies in 1586 karyotypes and relation to sperm parameters». Human Reproduction 17: 2600-2614.
- ↑ Yukiko, Katagiri; Queenie V Neri, Takumi Takeuchi, Peter N Schlegel, Wael A Megid, Marijo Kent-First, Zev Rosenwaks, Gianpiero D Palermo (2004). «Y chromosome assessment and its implications for the development of ICSI children». Reproductive BioMedicine Online 8 (3): 307-318. doi:10.1016/S1472-6483(10)60911-X.